MTHFR, MTR, MTRR, TCN w zespole Downa czyli o homocystynurii
styczeń 19, 2015 by Jarek
Kategoria: Wiedza o Zespole Downa
Homocystynuria to stan, który rozpoznaje się dość łatwo po bardzo wysokim poziomie homocysteiny i po stanie oka. Są to typowe objawy dla tzw. klasycznej homocystynurii, która jest efektem mutacji genu CBS. W efekcie mamy zaburzenia metabolizmu aminokwasów zawierających siarkę.
Zaczynamy od wikipedii.org i definicji problemu http://pl.wikipedia.org/wiki/Homocystynuria
Homocystynuria (ang. homocystinuria) – heterogenna etiologicznie, uwarunkowana genetycznie choroba metaboliczna, polegająca na nieprawidłowym metabolizmie aminokwasu metioniny. Homocystynuria charakteryzuje się podwyższonym poziomem homocysteiny w surowicy i w moczu. Najczęstszą postacią schorzenia jest homocystynuria spowodowana niedoborem i niską aktywnością enzymu syntazy β-cystationionowej (ang. cystathionine beta synthase deficiency), który katalizuje reakcję przekształcenia homocysteiny do cysteiny poprzez cystationinę. Reakcja katalizowana przez syntazę β-cystationionową wymaga udziału pirydoksyny (witaminy B6), dlatego w części przypadków homocystynurii obserwuje się poprawę po uzupełnieniu niedoboru pirydoksyny. Znanych jest dodatkowo przynajmniej siedem innych, znacznie rzadszych chorób genetycznych powodujących podobny blok metaboliczny; aby odróżnić niedobór CBS od tych rzadszych przyczyn używa się terminu klasycznej homocystynurii albo homocystynurii z powodu niedoboru syntazy β-cystationionowej. Dziedziczenie choroby jest autosomalne recesywne, obydwa allele genu CBS muszą być zmutowane, aby homocystynuria ujawniła się klinicznie. Heterozygotyczni nosiciele mutacji w jednym allelu genu CBS nie chorują. Ryzyko urodzenia kolejnego dziecka z homocystynurią wynosi 25%.
Odpowiednio wczesne wdrożenie leczenia i jego dożywotnie kontynuowanie pozwala na prawidłowy rozwój umysłowy chorych i uniknięcie obniżających jakość życia powikłań.
W zespole Downa tego typu, klasyczna wersja homocystynurii nie jest odnotowywana. Jest to efekt potrojenia genu CBS znajdującego się na 21 chromosomie i jego nadaktywności.
“…we show that the levels of CBS in DS brains are approximately three times greater than those in the normal individuals”
http://www.ncbi.nlm.nih.gov/m/pubmed/16274669/
Jednakże analizując przypadki leukemii i mutacji genu CBS, to należy potwierdzić, że ten gen i jego mutacje są ściśle związane z rodzeniem dzieci z ZD i tym, że to one mają leukemię http://www.nature.com/leu/journal/v16/n11/full/2402705a.html. Może to jednak oznaczać konieczność sprawdzania tej mutacji u dzieci z ZD w połączeniu z badaniem na funkcjonowanie witaminy B 6.
http://www.ashg.org/2014meeting/abstracts/fulltext/f140121610.htm
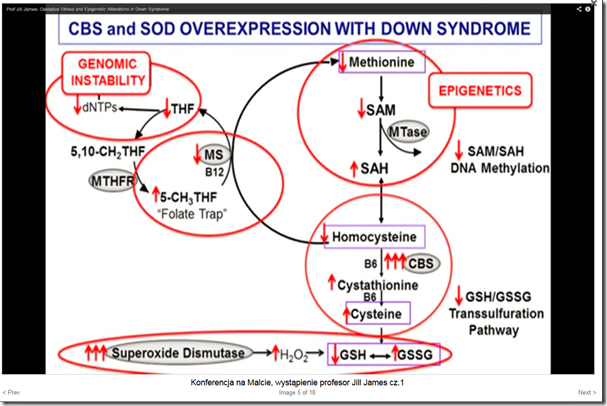
Proponuję teraz wrócić do znanych nam tematów z wykładu Jill James dotyczących cykli kwasu foliowego, SAM, cysteiny.
http://www.zespoldowna.info/konferencja-na-malcie-wystapienie-profesor-jill-james-cz-1.html
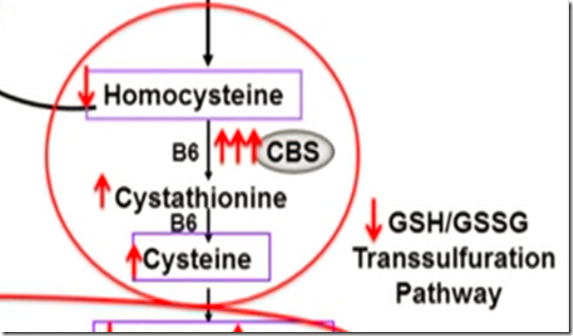
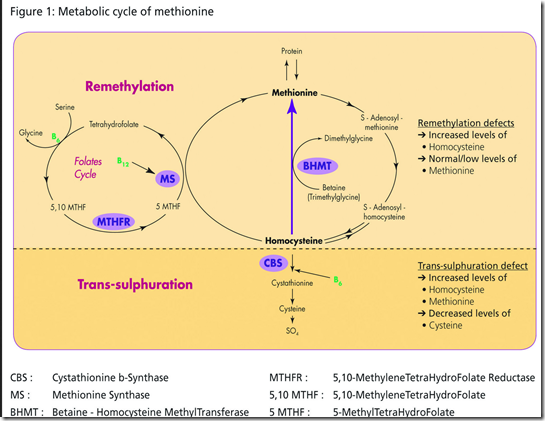
Na tym slajdzie mamy zaprezentowany cały przebieg procesów w ZD. Dla homocystynurii klasycznej istotna jest ta część, gdzie gen CBS wpływa na remetylację homocysteiny. Jak widać na diagramie, nadaktywność CBSu powoduje znaczący spadek homocysteiny. Nie odnotowałem przypadku, by było inaczej, a nie ma w literaturze doniesienia, by dziecko z ZD miało gen CBS zmutowany na wszystkich trzech jego kopiach i aby one mogły mieć taki wpływ jak to jest opisywane w klasycznej wersji tej choroby.
Zatem w ZD jedynymi czynnikami mającymi wpływ na poziom homocysteiny mogą być geny biorące udział w cyklach powiązanych z cyklem cysteiny.
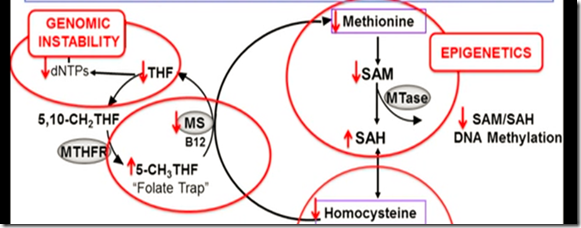
Jill James na swoim diagramie wskazywała pewną część genów, których praca zmieniona w efekcie mutacji (znajdują się one na innym chromosomie niż 21) ma istotny wpływ na funkcjonalność tych cykli. Są to geny:
-MS (methionine synthase), który najczęściej jest nazywany jako MTR
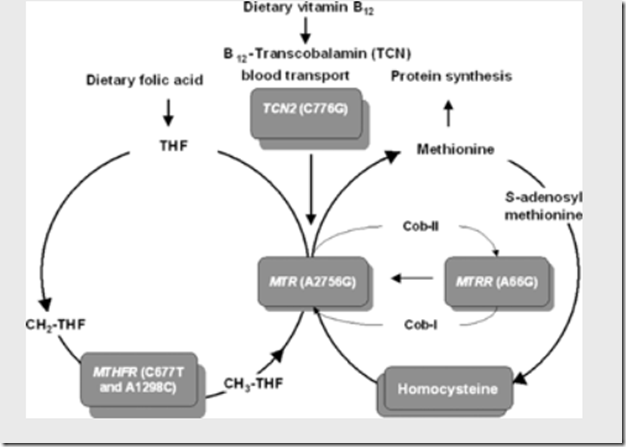
Popatrzmy teraz na ten diagram z Nature. Pokazuje on bardziej szczegółowo geny wpływające na cykl i jak są one powiązane z określonymi witaminami z grupy B.
http://www.nature.com/ajg/journal/v103/n2/fig_tab/ajg20085077f1.html
Mamy zatem geny i ich mutacje:
MTHFR C 677 T i MTHFR A 1298 C
witaminy istotne: B 2 i B 9
mutacje tego genu powodują, że enzymy przez niego produkowane są nieaktywne, źle funkcjonują, a bez tego nie można przekształcić homocysteiny w metioninę
MTR A 2756 G
witaminy istotne: B 12
mutacje tego genu wpływają na wielkość enzymu methionine synthase, który jest bardzo mały i nieefektywny w procesach
MTRR A 55 G
witaminy istotne: B 12
mutacje powodują tworzenie się słabych i małych cząstek enzymu methionine synthase reductase, które po prostu nie funkcjonują
TCN 2 C776G
witaminy istotne: B 12
mutacja tego genu powoduje stały brak witaminy B 12
Ostatnie dwa geny na które należy zwrócić uwagę to gen BHMT oraz MMADHC .
BHMT (betaine homocysteine methyltransferase) jest pewnym “skrótem” w procesie przekształcania homocysteiny do poziomu metioniny. Jego złe działanie pod wpływem stresu, może prowadzić do homocystynurii.
http://www.cystadane.com/images/Metabolic%20cycle%20of%20methionine2.jpg
MMADHC to gen, który bierze udział w przekształcaniu witaminy B 12 w jedną z dwóch jej form.W momencie, gdy mutacja tego genu uniemożliwia wytwarzania jednej z jej form nazywanej metylkobalaminą (MeCbl) nie może dokonywać się przekształcenie homocysteiny w metioninę na poziomie funkcjonowania genu MTR.
WNIOSKI:
1.W zespole Downa homocystynuria związana może być głównie z trwałym deficytem witaminy B 12 lub uszkodzeniem tych mechanizmów, w którym bierze ona aktywny udział.
2.W zespole Downa w związku z silnym skojarzeniem jego występowania z mutacjami genu MTHFR, MTR, MTRR głównym problemem prowadzącym do homocystynurii jest istotne zaburzenie poziomu witamin z grupy B, w odpowiedniej formulacji, biorących udział w procesie metylacji: B 9, B 12, B 6, B 2 oraz choliny, która też należy do grupy witamin z tej grupy. także istotną rolę odgrywają betainy w postaci TMG.
http://www.zespoldowna.info/witamina-b-2-mutacja-mthfr-i-zespol-downa.html
http://www.zespoldowna.info/mthfr-c-677-t-zespol-downa-mtrr-a-66-g-mtr-a-2756-g.html
DIAGNOZA:
1.Konieczne jest zbadanie mutacji poszczególnych genów w następującej kolejności:
MTHFR
MTR
MTRR
TCN
BHTM
CBS.
2.Podałem taką kolejność ze względów finansowych i dostępności badań. Zakładam, że jeżeli uzyskamy wynik pozytywny na poziomie MTHFR to już będzie to sugestia do rozpoczęcia specjalnego leczenia w tym kierunku.
3.Badanie pozostałych mutacji może jedynie skutkować stwierdzeniem ile i jakiej witaminy B 12 powinniśmy stale podawać, tudzież wykluczyć mutacje na poziomie CBS i związanego z tym zaburzonym wchłanianiem witaminy B 6.
LECZENIE:
1.Protokoły lecznicze w tym wypadku powinny uwzględniać szybkie podanie witaminy B 12 w postaci zastrzyków
2.Następnie w zależności od mutacji genu należy dobrać odpowiednie dawki METYLOWANYCH wersji witamin B9, B 12, B6 oraz witaminy B 2 by utrzymywać ich obecność na odpowiednim poziomie dla tych procesów.
3.Betainy w postaci TMG są też tutaj wskazane
4.Dieta z dużym wskazaniem na wegetarianizm.
UWAGI DOTYCZĄCE ZESPOŁU DOWNA I POZIOMU HOMOCYSTEINY:
1.Potrojony gen CBS może powodować inny obraz choroby na poziomie ilości zmierzonej homocysteiny z krwi, czyli nie 20-30 tylko 10-15μmol/l .
2.DYRK 1 A, potrojony w ZD, także wpływa na obniżenie jej poziomu!!! http://www.ncbi.nlm.nih.gov/pubmed/19844572
3.Stymulacja genu DYRK 1 A poprzez podawanie EGCG może podnosić poziom homocysteiny.
PRZYDATNA LITERATURA:
http://geneticgenie.org/all-mutations/
http://www.rarediseases.org/docs/Homocystinuria_11_29b.pdf
http://ghr.nlm.nih.gov/condition=homocystinuria
http://ghr.nlm.nih.gov/gene/MMADHC
http://ghr.nlm.nih.gov/gene/MTR
http://ghr.nlm.nih.gov/gene/MTRR
http://ghr.nlm.nih.gov/gene/MTHFR