Prenatalna diagnostyka zespołu Downa
luty 6, 2010 by Jarek
Kategoria: Wiedza o Zespole Downa
Zaskoczyło mnie w tym jedno, że duża liczba osób, która pisze do mnie pyta się o prenatalną diagnostykę zespołu Downa. Myślałem, że wszystkim jest to wiadome, ale cóż jest pytanie, przygotowałem odpowiedź.
Przy opracowaniu tematu skorzystałem z:
http://www.genetyka-ginekolog.pl/diagnostyka_prenatalna/info.php
Diagnostyka prenatalna
Metody diagnostyki prenatalnej dzielą się na metody nieinwazyjne oraz metody inwazyjne.
Nieinwazyjne metody diagnostyki prenatalnej:
1. Ultrasonografia (USG).
2. Badania przesiewowe oparte na oznaczaniu specyficznych substancji pochodzenia płodowego obecnych w surowicy krwi matki.
3. Badanie komórek i DNA pochodzenia płodowego obecnych w krążeniu matczynym.
Inwazyjne metody diagnostyki prenatalnej:
1. Amniocenteza (amniopunkcja).
2. Biopsja kosmówki (biopsja trofoblastu).
3. Kordocenteza (pobieranie krwi płodowej ze sznura pępowinowego).
Cele diagnostyki prenatalnej:
1. Ocena stanu płodu w celu wyboru optymalnego momentu i sposobu rozwiązania ciąży.
2. W ciążach podwyższonego ryzyka genetycznego uspokojenie rodziców, że w aktualnie istniejącej ciąży dana wada rozwojowa lub choroba genetycznie uwarunkowana nie występuje u dziecka.
3. Wykrycie u płodu wad rozwojowych i chorób genetycznie uwarunkowanych, w przypadku których interwencja lekarska jeszcze w okresie życia wewnątrzmacicznego, stwarza szanse uratowania dziecka lub zmniejsza ryzyko powikłań okresu okołoporodowego.
4. Wykrycie u płodu wad wrodzonych, w których istnieje szansa uratowania dziecka pod warunkiem interwencji lekarskiej bezpośrednio po urodzeniu.
5. Wykrycie wad letalnych, nie dających szansy na przeżycie dziecka, a prowadzących do wewnątrzmacicznego obumarcia płodu lub zgonu dziecka w okresie około urodzeniowym.
BADANIA NIEINWAZYJNE
1) Ultrasonografia (USG)
USG płodu jest najczęściej stosowaną metodą diagnostyki prenatalnej. Zaleca się, aby przesiewowe badanie USG (tj. przeprowadzone u każdej ciężarnej kobiety) było wykonane przynajmniej 3-krotnie podczas trwania całej ciąży (kolejno między 11-14, ok. 20 oraz ok. 30 tygodnia ciąży). Szczegółowa i częstsza ultrasonografia wskazana jest w przypadkach podwyższonego ryzyka wystąpienia wrodzonej wady rozwojowej u dziecka lub zespołu wad wrodzonych. Jakość badania USG zależy od doświadczenia lekarza przeprowadzającego badanie i jakości aparatu jakim dysponuje.
Cele badania USG:
USG w 11-14 tygodniu ciąży – cele:
· Potwierdzenie wieku ciążowego
· Ocena żywotności płodu
· Ocena ilości płodów (z oceną kosmówkowatości)
· Wczesna diagnostyka dużych wad płodu
· Ocena przezierności fałdu karkowego (nuchal translucency, NT)
Przezierność fałdu karkowego, inaczej przezierność karokowa (NT) oceniana jest w badaniu USG między 11-14 tygodniem ciąży. Przeziernością karkową nazywamy obraz ultrasonograficzny, odpowiadający podskórnemu gromadzeniu się płynu w okolicy karkowej u płodu. Grubość fałdu karkowego rośnie wraz z wiekiem ciążowym, a tym samym długością ciemieniowo-siedzeniową CRL (ang. crown-rump length), która ściśle zależy od wieku ciąży.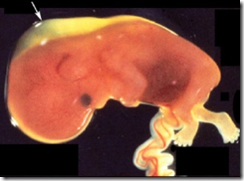
Począwszy od 14 tygodnia trudniej jest zmierzyć przezierność karkową (wierzchołkowa pozycja płodu), a prawdopodobieństwo uzyskania pomiaru spada z 98-100% do 90%. Na dodatek nie istnieje grupa kontrolna, do której można by było przyrównać otrzymane wyniki NT.
Przezierność karkowa – normy:
Opracowane normy NT obejmują ciąże od początku 11 Hbd do końca 13 Hbd (13 tyg. + 6 dni).
Dla CRL=45mm (11 Hbd) mediana wynosi 1,2 mm, a 95 centyl 2,1 mm.
Dla CRL=84mm (13+6 Hbd) mediana wynosi 1,9 mm, a 95 centyl 2,7 mm.
Ryzyko indywidualne obliczamy mnożąc wartość ryzyka wstępnego dla danej pacjentki (wynikającego z jej wieku oraz wieku ciążowego) przez różnicę między wartością NT zmierzoną a medianą dla danego CRL.
Przezierność karkowa – interpretacja:
Ryzyko wystąpienia aberracji chromosomowych i innych zaburzeń wrodzonych jest raczej związane z grubością niż z obrazem ultrasonograficznym fałdu karkowego. Skrining NT pozwala zidentyfikować około 72% płodów z zespołem Downa przy odsetku wyników fałszywie dodatnich wynoszącym 5%. W czasie 2 trymestru ciąży fałd karkowy ulega zazwyczaj wchłonięciu, a tylko w nielicznych przypadkach rozwija się obrzęk karku (ang. nuchal edema) lub tzw. cystic hygroma (obrzęk wielokomorowy szyi), którym może towarzyszyć uogólniony obrzęk płodu. Ryzyko wystąpienia trisomii u płodu rośnie wraz ze wzrostem przezierności (grubości) fałdu karkowego NT.
- NT = 3 mm – ryzyko trisomii podwyższone ponad ryzyko wynikające z wieku matki 3 razy
- NT = 4 mm – ryzyko trisomii podwyższone ponad ryzyko wynikające z wieku matki 18 razy
- NT = 5 mm – ryzyko trisomii podwyższone ponad ryzyko wynikające z wieku matki 28 razy
- NT > 5 mm – ryzyko trisomii podwyższone ponad ryzyko wynikające z wieku matki 36 razy

Wykres 1: Ryzyko urodzenia dziecka z trisomią 21 w zależności od wieku matki i wartości NT.
Poza aberracjami chromosomowymi istnieją inne przyczyny zwiększenia grubości fałdu karkowego. Są to:
1) niewydolność płodowego układu krążenia związana z wadą serca i/lub dużych naczyń
2) zastój krwi żylnej w obrębie głowy i szyi płodu spowodowany uciskiem
3) nieprawidłowy lub opóźniony rozwój układu limfatycznego
4) nieprawidłowy drenaż limfatyczny w chorobach nerwowo-mięśniowych płodu
5) anemia płodowa lub hipoproteinemia
6) infekcje płodu powodujące anemię lub niewydolność krążenia
7) zmieniony skład substancji międzykomórkowej
Innym markerem ultrasonograficznym aberracji chromosomowych (przede wszystkim Z. Downa) jest brak lub niedorozwój kości nosowej u płodu – NB (ang. nasal bone). Obecność kości nosowej zaznaczana jest w opisie badania USG jako NB (+), a brak jako NB(-). Brak kości nosowej stwierdza się:
- u 67 % płodów z trisomią 21
- u 55 % płodów z trisomią 18
- u 34 % płodów z trisomią 13
- u 11 % płodów z monosomią X (Zespół Turnera)
- u 7 % płodów z triploidią
Oprócz pomiaru NT, w trakcie badania USG w 11-14 Hbd możliwa jest również ocena anatomii płodu i ewentualne wykrycie wrodzonych wad rozwojowych dziecka. Stwierdzenie niektórych wad wrodzonych, powinno nasuwać podejrzenie aberracji chromosomowej u płodu i jest wskazaniem do wykonania inwazyjnej diagnostyki prenatalnej z oceną kariotypu płodu. Poniżej wymieniono kilka z nich:
- zespół Dandy’ego-Walkera (częstość 1/30.000) – aberracje chromosomowe w 40% przypadków; ponadto występuje w 50 zespołach genetycznych
(Z. Dandy’ego-Walkera: zanik robaka móżdźku, zwężenie komory IV, powiększenie cysterna magna)
- brak ciała modzelowatego (częstość 1/1000) – występuje w ok. 100 zespołach genetycznych w tym w trisomii 13 i 18
- cystic hygroma: 75% aberracje chromosomowe (głównie zespół Turnera)(oubstronne, torbielowate struktury w okolicy potyliczno-szyjnej płodu)
- wentrykulomegalia: (częstość 1/1000) – w 10% wiąże się z aberracją chromosomową
- holoprosencefalia: (częstość 1/10.000) – w 30% aberracje chromosomowe (trisomia 13 i 18)
- małogłowie: (częstość 1/1000) – w 15% aberracje chromosomowe (trisomia 13, delecje 4p i 5p)
- przepuklina przeponowa: (częstość 1/3000) – 20% aberracje chromosomowe
- omphalocoele (przpuklina sznura pępowinowego): (częstość 1/3000) – w 60% aberracje chromosomowe – * ryzyko aberracji jest większe, jeśli przepuklina pojawia się wcześniej oraz jeśli zawiera tylko jelita
- gastroschisis (wytrzewienie): (częstość 1/5000) – rzadko wiąże się z aberracjami chromosomowymi
- wady serca: (częstość 5-10/1000) – aberracje chromosomowe w 5% przypadków
- zarośnięcie przełyku: (częstość 1/3000) – w 4% aberracje chromosomowe
- zarośnięcie dwunastnicy: (częstość 1/5000) – 40% aberracje chromosomowe (głównie trisomia 21)
- hiperechogeniczne jelita: (częstość 1/200) – ryzyko trisomii 21 wzrasta 20-krotnie
- hipotrofia płodu: w 1% przypadków aberracje chromosomowe (trisomia 21, triploidia)
- wodonercze: w 3% wiąże się z aberracjami chromosomowymi
- megacystis (pęcherz olbrzymi): w 20% aberracje chromosomowe, ale w 50% samoistnie zanika
Ryzyko aberracji chromosomowej wzrasta wraz z ilością wad rozwojowych stwierdzanych u płodu. I tak w przypadku stwierdzenia 2 wad rozwojowych, ryzyko aberracji chromosomowej u dziecka wynosi średnio ok. 10%, w przypadku 3 wad – ok. 30%, 4 wad – 50%, 5-7 wad – 60-70%, 8 lub więcej – ok. 90%.
2) Badania przesiewowe surowicy krwi matki
I trymestr ciąży:
Badania przesiewowe w 1. trymestrze (test PAPP-A):
1. Wolna podjednostka beta-hCG
2. PAPP-A
Test PAPP-A wraz z pomiarem NT (wykonywane między 11 a 14 tygodniem ciąży):
- dla trisomii 21 (tzn. zespołu Downa) – wykrywalność wynosi 86,3%, przy odsetku wyników fałszywie dodatnich równym 5%
- dla wszystkich aberracji chromosomowych wykrywalność sięga 90%, przy 6% wyników fałszywie dodatnich
Polegają na oznaczeniu markerów biochemicznych w surowicy krwi kobiet ciężarnych:
- Alfa-fetoproteina (AFP)
- Podjednostka beta ludzkiej gonadotropiny kosmówkowej (beta-hCG)
- Nieskoniugowany estriol (uE3)
- PAPP-A
- Inhibina A
· białko PAPP-A – niższe stężenie w ciąży z trisomią 21
II trymestr ciąży:
Test potrójny (wykonywany między 15 a 19 tygodniem ciąży):
Test potrójny to badanie, które polega na określeniu stężeń podjednostki beta-hCG, alfa-fetoproteiny (AFP) i nieskoniugowanego estriolu (uE3). Wykrywa ono 50-75% ciąż z trisomią 21 (zespołem Downa), a fałszywie dodatnie wyniki otrzymuje się w 5% przypadków. Przy uwzględnieniu NT, wykrywalność sięga 85-90% przy odsetku wyników fałszywie dodatnich wynoszącym 5%.
Poniżej opisano patologie ciąży, w jakich obserwuje się wzrost lub spadek stężeń markerów biochemicznych, badanych testem potrójnym.
· podjednostka beta-hCG – wyższe stężenie w ciąży z trisomią 21, zaśniadzie groniastym, ciąży mnogiej;
- niższe stężenie w ciąży z trisomią 18, ciąży obumarłej
· nieskoniugowany estriol (uE3) – niższe stężenie w ciąży z trisomią 21, bezmózgowiem, aplazją lub hipoplazją nadnerczy
· AFP
Patologia płodu, w której podwyższone jest stężenie AFP w surowicy:
1) otwarte wady cewy nerwowej
2) ubytki ściany brzucha
3) cystic hygroma
4) atrezja przewodu pokarmowego
5) niektóre wady układu pokarmowego
6) choroby skóry (epidermolysis bullosa simplex, aplasia cutis congenita)
7) IUGR
Inne przyczyny matczyno-płodowe wzrostu AFP w surowicy:
- ciąża mnoga, ciąża obumarła, wady łożyska lub pępowiny, immunizacja Rh
Choroby matki, w których podwyższone jest stężenie AFP:
- guzy wątroby, ostre zapalenie wątroby
Wykres 2: Wartości stężeń AFP w surowicy krwi matki w trzech grupach pacjentek ciężarnych – matek zdrowych płodów (unaffected), matek płodów z zespołem Downa (Down syndrome) i matek płodów z otwartą wadą cewy nerwowej (open spina bifida).
3) Komórki i DNA pochodzenia płodowego we krwi kobiety ciężarnej
We krwi ciężarnych krąży pewna ilość komórek płodowych (komórki trofoblastu, pierwotne erytrocyty jądrzaste, granulocyty) dostępnych badaniu. Ograniczeniami metody są jednak mała ilość komórek pochodzenia płodowego we krwi ciężarnej oraz trudności w odróżnieniu komórek matczynych od komórek płodowych.
Odsetek komórek pochodzenia płodowego w pobranej próbce krwi kobiety ciężarnej może zostać zwiększony poprzez zastosowanie metod automatycznego sortowania komórek: MACS (magnetic cell sorting) lub FACS (fluorescence activated cell sorting). Na uzyskanych komórkach można następnie przeprowadzać badania cytogenetyczne techniką FISH. Czułość metody podobna jest do czułości biochemicznych testów przesiewowych, ale badanie jest kosztowne i pracochłonne.
We krwi kobiet ciężarnych występują także niewielkie ilości wolnego DNA pochodzenia płodowego, który może być wykorzystany do badań genetycznych techniką PCR. Obydwie wymienione metody nie weszły jeszcze do rutynowej diagnostyki i są w trakcie udoskonalania.
METODY INWAZYJNE
1) Amniopunkcja (amniocenteza)
Amniopunkcja – informacje ogólne:
- wykonywana jest między 15-18 tygodniem ciąży
- pobranie 15-20 ml płynu owodniowego
- ryzyko utraty ciąży (poronienia) w związku z badaniem wynosi 0,5-1%
- czas oczekiwania na wynik: 10 dni – 3 tygodnie
Amniocenteza jest możliwa do wykonania także między 10 a 14 tygodniem ciąży (amniocenteza wczesna), ale wówczas ryzyko poronienia wzrasta do 2%, a ryzyko wystąpienia wad kończyn (m. in. stóp końsko-szpotawych u płodu) jest wysokie. Dlatego też wczesna amniocenteza wykonywana jest bardzo rzadko.
Amniopunkcja – wskazania:
1) Podwyższone ryzyko urodzenia dziecka z aberracją chromosomową:
- wiek ciężarnej powyżej 35 lat (zazwyczaj bierze się pod uwagę wyniki badań przesiewowych i na ich podstawie weryfikuje wyjściowe ryzyko wynikające z wieku matki i dopiero wówczas podejmuje decyzję o wykonaniu amniopunkcji)
- urodzenie dziecka z aberracją chromosomową z poprzedniej ciąży
- nosicielstwo translokacji lub innej aberracji chromosomowej u jednego z rodziców
- stwierdzenie w USG patologii płodu sugerującej występowanie aberracji chromosomowej
- nieprawidłowy wynik testów biochemicznych (test PAPP-A, test potrójny) – ryzyko aberracji u płodu >1:200
2) Urodzenie dziecka z wadą cewy nerwowej z poprzedniej ciąży
2) Biopsja kosmówki
Biopsja kosmówki (CVS – z ang. chorionic villus sampling) – informacje ogólne:
- wykonywana jest między 10-14 tygodniem ciąży
- pobranie 5-10 g tkanki
- oczekiwanie na wynik 1-3 tygodnie (komórki trofoblastu aktywnie się dzielą, dzięki czemu możliwa jest bezpośrednia analiza chromosomów oraz szybkie badania biochemiczne i molekularne)
- ryzyko poronienia około 2 %
Stwierdzono związek między biopsją kosmówki wykonywaną przed 10 tygodniem ciąży, a występowaniem wad ubytkowych kończyn płodu oraz niedorozwojem żuchwy i języka.
Biopsja kosmówki – wskazania:
- podobne jak w przypadku amniocentezy z wyjątkiem podwyższonego ryzyka urodzenia dziecka z wadą cewy nerwowej
- CVS jest metodą z wyboru w przypadku molekularnej diagnostyki prenatalnej chorób monogenowych
3) Kordocenteza
Kordocenteza – informacje ogólne:
- wykonywana od 17 tygodnia ciąży do momentu porodu
- pobranie 0,5-1,0 ml krwi płodu z żyły pępowinowej
- ryzyko poronienia ok. 1,0-1,5%
- istnieje ryzyko zanieczyszczenia krwią matki i otrzymania błędnego wyniku kariotypu płodu
Kordocenteza – wskazania:
- wykrycie w USG po 18. tygodniu ciąży wad sugerujących możliwość aberracji chromosomowych u płodu
- uzyskanie materiału do badań cytogenetycznych (np. weryfikacja mozaikowatości) lub badań molekularnych
- diagnostyka i leczenie konfliktu serologicznego, ocena morfologii krwi płodu (np. małopłytkowość)
- diagnostyka prenatalna genetycznie uwarunkowanych chorób krwi (anemia sierpowatokrwinkowa)
PRENATALNA OCENA KARIOTYPU
Wskazania do prenatalnej oceny kariotypu wymieniono przy opisie amniopunkcji.
Aktualnie podstawą badań cytogenetycznych w diagnostyce prenatalnej (ocena kariotypu płodu) jest hodowla komórek płynu owodniowego uzyskanych na drodze amniopunkcji lub hodowla komórek trofoblastu. Uzyskuje się preparaty cytogenetyczne i ocenia kariotyp płodu z zastosowaniem klasycznych technik prążkowych.
Prążkowanie chromosomów jest od ponad 30 lat stosowane z powodzeniem jako główna metoda prenatalnej diagnostyki cytogenetycznej. W celu analizy kariotypu wykorzystuje się takie techniki prążkowe jak GTG (trawienie trypsyną i barwienie odczynnikiem Giemsy), R (ang. reverse banding, prążkowanie odwrotne), Q (prążkowanie z zastosowaniem fluorochromu kwinakryny) oraz T. Rozdzielczość technik prążkowych wynosi od 5 do 10 milionów par zasad.
Namnożenie komórek trofoblastu lub amniocytów w hodowli in vitro, przygotowanie preparatów i analiza cytogenetyczna chromosomów jest procesem czasochłonnym. Wynik badania otrzymuje się średnio od 10 dni do trzech tygodni po pobraniu materiału.
Nowoczesne metody badań cytogenetycznych w diagnostyce prenatalnej
Rozwój współczesnej diagnostyki prenatalnej stał się możliwy dzięki osiągnięciom w dziedzinie cytogenetyki molekularnej i biologii molekularnej:
FISH (fluorescencyjne hybrydyzacja in situ):
· stosowana od lat 80-tych XX wieku
· obok analizy chromosomów umożliwia także badanie jąder w stadium interfazy
· zastosowanie sond specyficznych (dostępnych komercyjnie) dla chromosomów pary 13, 18, 21, X i Y umożliwia szybką diagnostykę najczęściej występujących aneuploidii chromosomowych
· wymaga pozyskania niewielkiej ilości amniocytów bądź komórek kosmówki
· wyniki badania uzyskuje się w przeciągu 24 godzin
Array-CGH (porównawcza hybrydyzacja genomowa z wykorzystaniem mikromacierzy):
· DNA pacjenta (wyizolowany z amniocytów płynu owodniowego) i DNA referencyjny (kontrolny) wyznakowane na różne kolory są hybrydyzowane do płytek mikromacierzy zawierających fragmenty genomowego DNA
· umożliwia detekcję niewielkich zmian ilościowych (duplikacje, delecje) w obrębie chromosomów pacjenta
· wysoka rozdzielczość (1 mln – 500 tys. par zasad)
Detekcja aneuploidii chromosomowych z wykorzystaniem technik biologii molekularnej:
QF-PCR (ilościowy, fluorescencyjny PCR):
· fragmenty DNA (powtórzenia mikrosatelitarne) podlegają amplifikacji, znakowaniu fluorescencyjnemu a ilość kopii mierzona jest podczas rozdziału elektroforetycznego
· umożliwia szybką detekcję aneuploidii chromosomowych z wykorzystaniem DNA wyizolowanego z amniocytów lub komórek kosmówki
· technika umożliwia również identyfikację przypadków disomii jednorodzicielskiej (UPD)
MLPA (ang. Multiplex Ligation-dependent Probe Amplification )
- metoda oparta o reakcję ligacji odpowiednich sond połączoną z reakcją amplifikacji.
- polega na amplifikacji nie łańcucha DNA, lecz sondy dodawanej do badanej próbki. Pojedyncza sonda zawiera dwa różne oligonukleotydy, z których każdy wiąże się ze starterem PCR. Każda z sond wiąże się specyficznie z wybranym miejscem sekwencji. Tylko w ten sposób połączone sondy ulegają amplifikacji w reakcji PCR. Liczba otrzymanych w wyniku reakcji PCR sond zależy od liczby odpowiadających sekwencji w badanym DNA.
- pozwala na równoczesną ocenę ilościową obecności ilości kopii wieloeksonowych genów. Na podstawie zmian stosunków ilościowych poszczególnych fragmentów można wnioskować o delecjach bądź duplikacjach odpowiednich odcinków genów.
- zaletą tej metody jest prostota wykonania, niska cena i mała ilość DNA potrzebna do jej wykonania.
Piśmiennictwo:
Nicolaides K.H., Węgrzyn P.: Badanie ultrasonograficzne między 11-13 tygodniem ciąży. Fetal Medicine Foundation, London 2004.
Down syndrome, or trisomy 21, is a chromosome irregularity caused by a genetic mutation in one in every 800 live births in all races and economic groups.
It is also the most frequent genetic cause of mild to moderate mental retardation and associated medical problems, and while people with Down syndrome are able to lead fulfilling and productive lives, there are many associated medical problems.
Individuals with the syndrome have a lower than average cognitive ability – often ranging from mild to moderate developmental disabilities – and often have problems registering and communicating coherent speech. A smaller number of sufferers have severe to profound mental disability.
Other health concerns for individuals with Down syndrome include a higher risk of congenital heart defects, recurrent ear infections, gastroesophageal reflux disease, thyroid dysfunctions, sleep apnea, and higher risk of spinal injury.
Individuals with the syndrome are identifiable by a number of physical characteristics, especially facial, including microgenia (a smaller than average chin), a very rounded face, macroglossia (protruding or oversized tongue), an epicanthic fold of the eyelid, up- slanting palpebral fissures (the separation between the upper and lower eyelids), a simian crease (a single instead of a double crease across one or both palms), a larger than normal space between the big and second toes, shorter limbs, poor muscle tone, and a higher propensity to be overweight.
Degrees of the disability vary, however, and while some individuals are very physically disabled, others are very able and even athletic. Similarly, degrees of mental disability vary, and the speed at which one can learn and complete tasks varies person to person.
It may difficult for some people with Down syndrome to complete simple tasks, such as feeding themselves, but others can perform more complex tasks, such as competitive sports, arts and dance.
While individuals with the genetic condition often have difficulties with verbal short-term memory, recent studies by Francis Connors and colleagues in the UK show that parental training programs can improve the working memory of those with Down syndrome.
It is therefore important for those with the syndrome to be in challenging and stimulating environments to allow their cognitive functions to improve, rather than deteriorate.


Prowadzę DIETETYCZNIE pacjentkę ze znacznym ryzykiem wystąpienia ch. Downa (13hbd; przezierność karku 80percentyl;1: 3 590). Od początku ciąży miała atopowe zapalenie skóry, które wcześniej u niej nie wystepowało. Azs zmniejsza się i znika na diecie, a zwiększa się po zejściu z zalecanej przeze mnie diety. Podejrzewam korelację: mniejsze zmiany azs=mniejsze ryzyko nieprawidłowych podziałów mitotycznych u płodu (zwykłym językiem:matka bez objawów=wieksze prawdopodobieństwo mniejszych zmian u płodu). Efekty, które widzę u pacjentki potwierdzają znaczne uwikłanie w produkty cukrogenne obojga rodziców wszystkich osób z ch. Downa(im niżej cukrogenna dieta tym lepsze funkcjonowanie naczyń w organizmie, a zatem prawdopodobny dobrostan mitotyczny). Zalecam 6 DNI OKROJONA DIETA DZIECKA DO ROKU (
specjalista laryngolog II st
Nr prawa wykonywania zawodu w Polsce : 3048372
Polecam wpisy Mamy Maciusia i Sylwizlodzi na forum: http://www.dobradieta.pl/forum/viewtopic.php?p=148420&highlight=#148420
obie to matki JUŻ NIE-AUTYSTYCZNYCH DZIECI. Dieta oprócz pracy z dzieckiem bardzo im i ich dzieciom pomogła. Chętnie służą radą. Dieta w ch. Downa jest taka sama jak dieta u dzieci z autyzmem. Zalecana przeze mnie dieta dziecka do roku (jednak bez ryżu, kukurydzy, prosa)jest w całości akceptowana przez Medycynę Akademicką. Wadliwy metabolizm omega 3 – 6 kwasów w ch. Downa i w autyzmie jest związany ze znaczącym przeładowaniem produktami cukrobennymi (zboża i produkty mleczne) i likwidacja pierwszych i rotowanie drugiej groupy (jadanie co 5-6 dni) powoduje, że ryba, jajko czy tłuszcz we frytkach, placku ziemniaczanym czy ziemniakach okraszonych olejem roslinnym zaczyna byc tolerowany. Zawsze polecam diete rozdzielną (osobno ryba osobno ziemniak; osobno jajko osobno ziemniak; osobno koltlet osobno ziemniaki) jako dobrze ukierowywującą na właściwie stosowaną dietę niżej węglowodanową. Im więcej zjemy weglowodanów tym bardziej jesteśmy zmęczeni, nie chce nam się uczyć, myśleć – chętniej wypoczywamy. Bywa też reakcja odwrotna – szczeg. u autystyków – nadpobudliwość po zbyt dużej dawce weglowodanów. Obiad: zupa jarzynowa/pomidorowa (z produktów z listy “cukrzyca”),kapuśniak, ogórkowa, rosół z ziemniakiem, ryba w sosie majonezowym, placek ziemnaczany, ziemniaki odsmażane, bitka ze schabu/kurczaka, bigos, kapusta z grzybami, surówka, bogracz BEZ MĄKI, gołąbki BEZ RYŻU (ja do gołąbków wrzucam tartą kapustę, jarzyny), fasolka po bretońsku BEZ MĄKI, pieczarki na oleju/maśle? Słonecznik na kolację? kalafior z oliwą? ziemniak/kluski ziemniaczane (BEZ DODATKU MĄKI) okraszony skwarkami/masłem? Frytki? Zupa z obiadu? Potrawy należy wybierać takie by dziecku smakowały. Jest co jeść nie bójmy się diety dziecka do roku życia – niekoniecznie na śniadanie trzeba zjeść płatki z mlekiem czy chleb/bułkę z serem.
Dzień dobry. W ciąży test Papa wykazał u mnie nieprawidłowy wynik beta-hCG, wskazujący na wysokie ryzyko zespołu Downa. Wynik pogorszył fakt mojego wieku czyli 41 lat. Amniopunkcja wykazała brak wad genetycznych. Dziecko urodziło się zdrowe. Moje pytanie: co mogło wpłynąć na nieprawidłowy wynik? Choruję na insulinoodporność, przed ciążą miałam stan przedcukrzycowy, w ciąży cukrzycę ciążową. Zarówno przed ciążą jak i w ciąży miałam epizody depresji. Ciąża była nieplanowana, więc nie znam wyników sprzed ciąży. W wieku 34 lat lekarka oświadczyła mi, że coś powoduje u mnie bezpłodność, założyliśmy z mężem, że już nie jesteśmy zdolni począć dziecka. Przed ciążą oboje sporo schudliśmy, zaczęliśmy dbać o zdrowie, zmieniliśmy styl życia na bardziej aktywny. Pytanie nr 2: Czy naprawdę taka zmiana jak dieta, spadek wagi plus bieganie, mogło coś u nas odblokować i staliśmy się nagle płodni?
PPA nie jest markerem godnym zaufania. Jest elementem statystyki. Wasza zmiana na pewno wpłynęła na Waszą płodności dzięki lepszy zdrowiu.