TREM2 znajduje się na 6 chromosomie i jest uważany za jeden z kluczowych genów w rozwoju choroby Alzheimera w zespole Downa.
Długo nie musieliśmy poczekać na potwierdzenie tezy o deregulacji funkcjonowania genów z poza 21 chromosomu. To dzięki temu, że MAMY BADANIA NAD ZESPOŁEM DOWNA I CHOROBĄ ALZHEIMERA, robimy krok dalej w stosunku do tego gdzie byliśmy. Jeszcze 4 lata temu wskazywałem na to, że tak może być, dziś nikt już nie wątpi, że ZD “ciągnie” dysfunkcyjnie geny z innych chromosomów.
Warto wrócić do tych ostatnich artykułów:
http://www.zespoldowna.info/zespl-downa-jest-zaburzeniem-ukladu-odpornosciowego.html
I znów zacznę od kluczowych zdań:
Nic w badaniach nad zespołem Downa nie jest sensowne oprócz medycyny spersonalizowanej.
Interferony to cząsteczki wytwarzane przez komórki w odpowiedzi na infekcję wirusową lub bakteryjną. U typowej osoby interferony są aktywowane tylko wtedy, gdy zwalczają infekcję. U osób z zespołem Downa odpowiedź interferonu wydaje się być stale aktywowana, co może predysponować je do zaburzeń autoimmunologicznych i białaczki, a być może nawet do choroby Alzheimera.
Z tych zdań możemy wyciągnąć jeden wniosek: ZD jest zaburzeniem odporności, która różnicuje się w sposób zindywidualizowany, co wynika z dziedziczonych genów od rodziców. Zatem nie tylko geny z 21 chromosomu decydują o rozwoju kaskad choroby Alzheimera, która w ZD ma typowy neuroinflamacyjny i odpornościowy charakter.
Wczoraj dotarła do mnie kolejna w tym kontekście kluczowa informacja: gen zlokalizowany na chromosomie 6p21.1 o nazwie TREM2 jest głównym czynnikiem rozwoju patologii choroby Alzheimera w ZD! O tym mówią BADANIA prowadzone w Wielkiej Brytanii.
https://en.wikipedia.org/wiki/TREM2
https://www.ncbi.nlm.nih.gov/pubmed/29278889/
WNIOSKI Z BADANIA:
1.Poziom białek TREM2 spada wraz z upływem wieku u osób z ZD.
2.Wykazano, że TREM2 bierze udział w fagocytozie czerwonych krwinek
3.Obwodowe TREM2 pochodzące z komórek erytromieloidalnych znacząco determinuje neuropatologię choroby Alzheimera u osób z ZD
4.Polimorfizm TREM2 R47H jeżeli występuje daje skrajną wersję choroby Alzheimera u osób z ZD.
Wyjaśnienia:
1.Dla mnie wbrew pozorom kluczowym tematem jest tutaj pojawienie się kwestii polimorfizmów. W Polsce nasi “profesjonaliści” wciąż odrzucają ich wpływ, ba nawet istnienie. Tutaj mamy badanie, które jako pierwsze obejmuje aktywność genu w wersji prawidłowej i z polimorfizmami homozygotycznymi, które pogarszają obraz patologii.
https://molecularneurodegeneration.biomedcentral.com/articles/10.1186/s13024-016-0137-9
2.Bardzo istotne jest po raz kolejny podkreślenie, że wszystko ma swój początek w zaburzeniu odporności wywołanej przez różne błędne mechanizmy.
3.Bardzo ważne jest to, że o ile w przypadku genu IL-6, czy IL-2 wspominano o możliwych i ich negatywnych oddziaływaniach, a nie są zlokalizowane na 21 chromosomie, to tutaj wyraźnie i jednoznacznie podkreślono fakt, że gen TREM2 pochodzi z innego chromosomu niż ten 21!
4.Co do samego genu TREM2, to jego polimorfizm homozygotyczny jest związany z bardzo szybkim pojawieniem się demencji. Jego polimorfizm TREM2 R47H, który jest ściśle związany ze zmianą odporności, jest czynnikiem zwiększającym ryzyko wystąpienia choroby Alzheimera między 2 – 4 krotnie. Co prawda nie wspomina się o nowo odkrytym polimorfizmie TREM2 H157Y, ale ten wariant także prowadzi do przyspieszonej choroby Alzheimera.
https://www.sciencedaily.com/releases/2017/08/170830094213.htm
5.Główną funkcją TREM2 jaka jest analizowana w chorobie Alzheimera, to odpowiedź mikroglia (mikrogleju) w mózgu na odkładanie się amyloidu beta i jego czyszczeniem z komórek. TREM 2 ma istotny wpływ na to jak działa mikroglej.
https://www.nature.com/articles/nrn.2016.7
http://www.alzforum.org/news/research-news/enter-new-alzheimers-gene-trem2-variant-triples-risk
http://www.zespoldowna.info/choroba-alzheimera-dwa-oblicza-mikrogleju.html
Mikroglej stanowiący około 5-20% populacji komórek nieneuronalnych w mózgu występuje w warunkach normalnych w formie spoczynkowej. Główne funkcje fizjologiczne mikrogleju sprowadzają się do monitorowania mikrośrodowiska tkanki, usuwania umierających neuronów i reakcji w wyniku stwierdzenia obecności obcego antygenu (Nakajima i in. 1993). W formie nieaktywnej mikroglej posiada liczne i długie rozgałęzienia części cytoplazmatycznej komórki. Ta specyficzna struktura prawdopodobnie ułatwia potencjalną reakcję tych komórek jako specyficznego dla tkanki nerwowej elementu układu immunologicznego.
Charakterystyczna transformacja mikrogleju z formy spoczynkowej do aktywowanej została poznana i opisana przez Rio Hortege prawie wiek temu. W wyniku aktywacji dochodzi do przemian morfologicznych którym towarzyszy: zwiększenie rozmiaru ciała komórki oraz obkurczenie rozgałęzień. Na poziomie molekularnym dochodzi do ekspresji białek adhezyjnych, reorganizacji cytoszkieletu oraz ekspresja elementów kompleksu zgodności tkankowej MHC typu I jak i II (Perry i in. 1987, 1989, Aloisi i in. 2000).
https://pl.wikipedia.org/wiki/Mikroglej
O roli mikrogleju z pewnością czytaliście przy okazji MHC tutaj: http://www.zespoldowna.info/zespl-downa-jest-zaburzeniem-ukladu-odpornosciowego-swietnie-a-jak-to-wytlumaczyc-lekarzowi-zeby-nie-kazal-szczepic-mojego-dziecka-z-zd.html
6.Z tej perspektywy patrząc jawi się następujący mechanizm choroby Alzheimera w ZD:
APOE4+TREM2 z jednej strony jako typologia i wpływ na nią genów RCAN1+DYRK1A+APP+SOD1+mir155 co pokazuje poniższy diagram zaprezentowany tutaj: http://www.alzforum.org/news/research-news/apoe-and-trem2-flip-microglial-switch-neurodegenerative-disease
7.Spadek aktywności TREM 2 wraz z wiekiem doprowadza do “odcięcia” energii dla mikrogleju, zatem następuje brak odpowiedzi komórkowej na uszkodzenie, działanie patogenu na komórkę. W efekcie prowadzi do jej śmierci. Ta reakcja jest ściśle z innymi błędnymi w ZD funkcjonującymi procesami kojarzonymi z IL-6, Il-2, Il-1, TNF w ZD.
http://www.alzforum.org/news/research-news/changing-times-disease-stage-alters-trem2-effect-tau
https://elifesciences.org/articles/20391
Aktywacja mikrogleju jaką wywołuje uszkodzenie tkanki związana jest ze wzrostem poziomu czynników o funkcji immunologicznej. W okresie tym może dojść do indukcji ekspresji szerokiej rzeszy receptorów powierzchniowych które przyspieszają odpowiedź immunologiczną. Pośród nich są receptory biorące udział w rozpoznawaniu cząsteczek związanych z patogenem, receptory komplementu (np. CR1, CR3, CR4), receptory cytokin (np. TNFRI, TNFRII, IL-1RI, IL-12R) oraz chemokin (np. CCR2, CCR3, CXCR4, CX3CR1) jak i receptory ułatwiające interakcje z układem immunologicznym jak np. z limfocytami T czy immunoglobulinami (np. Fc RI, RII, RIII) (Aloisi i in. 2001, Perry i in. 1992, Nakajima i in. 1993).
W wyniku uszkodzenia CNS napływowe monocyty oraz mikroglej zaczynają produkować również wiele związków prozapalnych takich jak cytokiny (IL-1,TNFα, IL-6, IL-12, IL-15, IL –18), chemokiny (IL-8, fraktalkina, IP-10, MIP-1α, MIP-1β, MCP-1, RANTES, MDC) oraz związki cytotoksyczne (iNOS, wolne rodniki tlenowe i azotowe) i prostanoidy (PGD2, PGE2, tromboksan B2) Aloisi i in. 2001). Rezultatem tego działania jest wzmożony napływ elementów krwiopochodnych z krwi obwodowej takich jak kolejna fala monocytów i makrofagów oraz limfocytów T i B, czy neutrofile. W pierwszej fazie odpowiedzi immunologicznej inicjowanej przez takie cytokiny jak IL-1, IL-6 czy TNF dochodzi do synergicznej reakcji monocytów, makrofagów oraz mikrogleju. Fakt ten wskazuje na współzależność tych komórek w efekcie uszkodzenia tkanki nerwowej.
Zwiększona proliferacja, migracja a przede wszystkim silna fagocytoza to cechy mikrogleju oraz makrofagów sprzyjające naprawie uszkodzonych części tkanki. Wzmożona proliferacja mikroleju w obrębie uszkodzenia jest efektem interakcji z uszkodzonymi neuronami jak również wynikiem skomplikowanych oddziaływań ze strony astrocytów oraz autostymulacji mikrogleju (Aloisi i in. 2001, Neumann i in. 2001, Dong i in. 2001). W wyniku kontaktu z uszkodzonym neuronem lub degenerującym połączeniem neuronalnym mikroglej wykazuje zdolność do transformacji w fagocyta – makrofaga mającego za cel usunięcie pozostałości z miejsca uszkodzenia tkanki nerwowej.
https://pl.wikipedia.org/wiki/Mikroglej
Interleukina 6 (IL-6) stanowi jedną z najważniejszych i najbardziej wielokierunkowo działających cytokin. Jest wydzielana głównie przez monocyty i makrofagi pod wpływem Interleukiny 1 i innych cytokin prozapalnych. Z jednej strony silnie pobudza procesy zapalne, ale także uczestniczy w zwrotnym hamowaniu wytwarzania TNF.
Spośród wielu różnych właściwości IL-6, najważniejsze to:
- stymuluje różnicowanie limfocytów B do komórek plazmatycznych
- aktywuje limfocyty T wraz z IL-1
- pobudza krwiotworzenie wykazując synergizm z Interleukiną 3
- jest czynnikiem pirogennym i stymuluje produkcję białek ostrej fazy.
https://pl.wikipedia.org/wiki/Interleukina_6
8. Jedynym środkiem terapeutycznym, który może wpłynąć na ten negatywny proces to znalezienie substancji wzmacniającej ilość TREM2, które w sposób efektywny mógłby zapobiegać odkładaniu się amyloidu beta i protein tau.
https://www.ncbi.nlm.nih.gov/pubmed/28393702
http://www.cell.com/neuron/fulltext/S0896-6273(17)30150-2
https://www.ncbi.nlm.nih.gov/pubmed/26949937
Możemy to na dzień dzisiejszy uzyskać działając pośrednio na TREM2 poprzez użycie resweratrolu, kurkumy via NF-kB i alpha-phenyl n-tert-butylnitrone PBN via TNF-α.



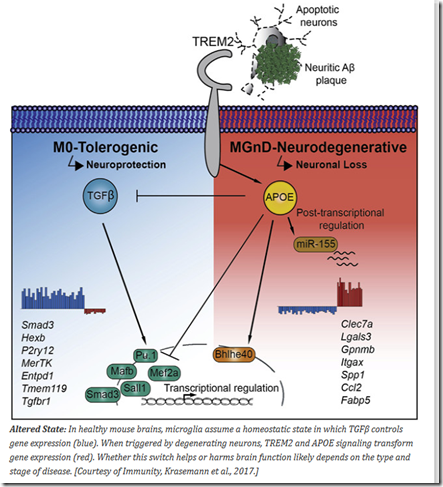
Według tych publikacji TREM2 jest inicjatorem choroby Alzheimera i jego regulacja może zablokować rozwój choroby. https://www.genengnews.com/gen-news-highlights/alzheimers-amyloid-gets-immune-system-trim/81255566