“Na swoim blogu bardzo dużo piszesz o kontrolowaniu homocysteiny, aby nie była za wysoka. A co w przypadku gdy jest za niska?”
czerwiec 4, 2020 by Jarek
Kategoria: MTHFR i inne polimorfizmy
Często mam wrażenie, że umawiacie się na zarzucenie nie mnie pytaniami na ten sam temat w tym samym momencie, mam takie wrażenie. Dzisiaj temat który został poruszony przez kilka osób: co się dzieje, gdy bez suplementacji mamy bardzo niską homocysteinę?
Niski poziom homocysteiny to dobrze czy źle?
Jeżeli mamy takie pytanie to zawsze musimy uściślić czym jest niski poziom homocysteiny. Dla mnie wartość poniżej 4,20 µmol/l bez suplementacji jest już takim sygnałem ostrzegawczym, ale poziom stały poniżej 3,80 µmol/l jest już momentem do wszczęcia alarmu. Dlaczego?
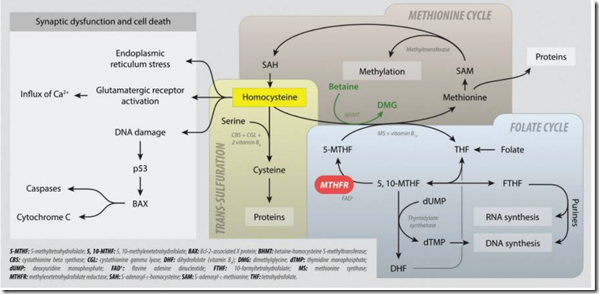
Niska homocysteina to w istocie informacja, że mamy mało metioniny, homocysteiny, cysteiny kluczowych aminokwasów dla metylacji i detoksu organizmu. Bez cysteiny nie ma przecież glutationu, a bez metioniny nie mamy SAM-e czyli kluczowego donoru grup metylowych w postaci s-adenozynometioniny. Niski poziom zatem może być takim samym problemem jak i nadmierny poziom.
Patrząc na przebieg procesu, zawsze w pierwszej kolejności sprawdzamy jaki jest poziom metioniny w naszej diecie. Jeżeli nie jesteśmy wegetarianami, to nie powinno być problemów. Potem ile mamy witaminy B12 i B9 plus kofaktorów…nie wspominając o cholinie. Analizujemy tutaj typowy efekt sprzężeń: zła dieta/niedobory żywieniowe-zapalenie-kacheksja
https://pl.wikipedia.org/wiki/Wyniszczenie
Jeżeli jednak to nie jest problemem, to przechodzimy dalej i analizujemy biomarkery które są mocno niedoskonałe mimo wszystko. Rezygnujemy z “łatwo dostępnych i statystycznych” na bardziej precyzyjne, czyli patrzymy na SAM i SAH oraz ich proporcje. Jeżeli to jednak wyklucza wady nerek to przechodzimy do genów.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4566450/
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2909276/
Zazwyczaj niski poziom homocysteiny łączy się z przyspieszonym, nadmiernie aktywnym genem CBS, w szczególności na jego allei CBS C699T. W ZD jest efektem potrojenia genu CBS przez co statystycznie dzieci z ZD mają przynajmniej o 1 µmol/l niższą homocysteinę, niż np. rodzeństwo bliźniacze. Jednak nie tylko to jest istotne. Musimy patrzeć na całą ścieżkę i kluczowe geny: AHCY, CBS, BHMT…ale i PDXK.
https://www.zespoldowna.info/czy-wiesz-ze-gen-cbs-potrzebuje-seryny-i-witamine-b6.html
https://www.zespoldowna.info/analiza-metylacji-cz-bhmt-i-cbs.html
https://www.zespoldowna.info/analizujemy-metylacje-cz-7-geny-cbssuox-nosbhmt.html
Jak to działa?
Zostawiamy na chwilę gen AHCY. Zakładamy, że s-adenozylohomocysteiny mamy dużo, w układzie dietetycznym homocysteiny także nam nie brakuje. Mamy gen CBS. Jego aktywność powoduje zaciągnięcie ponadnormatywnej ilości homocysteiny i obniżenie jej dostępności dla metylacji. Ta homocysteina ulega redukcji do poziomu cysteiny, a potem z kolei tytułem “podwojenia” genu CTH, ale potrojenia genu PDXK (tutaj oznacza to hamowanie), jest przepychana nie do wspaniałego glutationu, ale do produkcji substratów nie zawsze pożądanych takich jak np. amoniak.
https://en.wikipedia.org/wiki/Cystathionine_gamma-lyase
Jeżeli jeszcze mamy polimorfizmy genu BHMT następuje niejako dopchnięcie z kolana homocysteiny do przeróbki jej do poziomu cysteiny i w efekcie mamy bardzo niską homocysteinę.
Wracamy jednak do genu AHCY.
https://www.zespoldowna.info/ahcy-i-poziom-homocysteiny.html
Pozwolę sobie na cytat z powyższego wpisu:
Jaką rolę pełni gen AHCY? Jest genem odpowiedzialnym za degradację adenozylohomocysteiny na adenozynę i homocysteinę. Co oznacza, że homocysteina, która jest dostarczana do organizmu w diecie, potem jest remetylowana do postaci metioniny (dodana jest grupa metylowa) i służy jako podstawowy donor grup metylowych w postaci S-adenozylometioniny (SAMe), jest dzięki genowi AHCY znów homocysteiną. Oznacza to, że homocysteina jest stale obecna w organizmie i jej ilość jest też związana z funkcjonowaniem tego genu. jeżeli on będzie źle działał w organizmie będzie więcej metioniny, gdy będzie działał za szybko, będzie zbyt dużo homocysteiny. Jak to wygląda na wykresach, popatrzcie poniżej.
Po pierwsze spójrzmy na String. Ścieżka wzajemnych relacji z genem MAT1, BHMT, CBS, MTR jest oczywista i wynika z ze ścieżki metylacji. Geny te oddziaływują na siebie co jest oczywiste. Ściśle na efektywność tego genu oddziaływuje cała rodzina genów DNMT3 i vice versa. W ZD przypomnę mamy potrojony gen DNMT3L, który ściśle jest zależny od aktywności i działania genów DNMT3A i DNMT3B.
Innym czynnikiem wpływającym na efektywność pracy genu AHCY są metylotransferazy jak PNMT, HNMT, ASMT, GNMT, INMT i COMT (przykłady).
Jakie polimorfizmy są tutaj zagrożeniem?
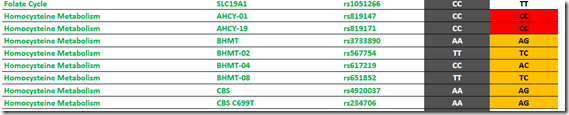
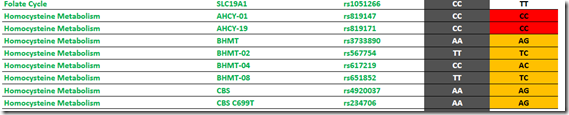
Według Amy Yasko musimy zwrócić uwagę na następujące polimorfizmy:
- rs819147 – AHCY-01 (Risk Allele: C)
- rs819134 – AHCY-02 (Risk Allele: G)
- rs819171 – AHCY-19 (Risk Allele: C)
Analizowane polimorfizmy są typologią spowolniającą proces i tworzącą blokadę konwersji adenozylohomocysteiny, przez co występuje zwiększona ilość metioniny, określana jako hypermetioniną. W efekcie cała metylacja jest wyhamowana i tworzą się nadmiary adenozylohomocysteiny, metylotransferazy nie otrzymują swoich grup metylowych negatywnie wpływając na replikację DNA, RNA, metylację białek i tłuszczy.
https://pubmed.ncbi.nlm.nih.gov/31957987/
https://pubmed.ncbi.nlm.nih.gov/30023284/
Gen AHCY w polimorfizmie zatem spowalnia konwersję prowadząc do niskiego poziomu homocysteiny…ale to często jest ukrywane polimorfizmem genu CBS!
Co zatem zrobić?
Wracamy do panelu.
Jeżeli mamy taki układ to krytycznym dla nas jest zbadanie SAM do SAH, czyli stwierdzenie: jaki wpływ ma gen AHCY na ilość dostępnej homocysteiny. Potem przestawiamy się na “spowolnienie” aktywności genu CBS i metylacji, poprzez podawanie produktów końcowych metylacji i przyspieszeniem pracy genu AHCY, by uzyskać odpowiedni efekt.
Postępowanie w przypadku wystąpienia tego polimorfizmu to:
-dieta nisko metioninowa
-suplementacja NAD+, witaminą NR
-inhibicja cyklu metioniny poprzez suplementację fosfatydylocholiną, kreatyniną i cysteiną
W przypadku regulacji CBS to witamina D3, seryna, witamina B6, apigenin.
W przypadku regulacji BHMT to cholina TMG i cynk.
Ważne są tutaj też działanie detoksykacyjne na poziomie amoniaku, co ciągnie za sobą analizę BH4 (bioptoryny) i funkcjonowania genów GCH1, MTHFRA1298C i kwasu foliowego, ale o tym już pisałem.
https://www.zespoldowna.info/bh4-polimorfizm-cgh1.html
Dzięki temu powinniśmy uzyskać regulację cyklu metylacji i podbić ilość dostępnej homocysteiny.


Dzień dobry, mam pytanie, jestem w ciąży ake wykonałam badanie homocysteiny i wynosi ona 3,3 µmol/l, kwas foliowy suplementowałam metylowany i zwykły w jednym preparacie. Jesli chodzi o MTHFR mam nastepujące mutacje: heterozygota A1289C i homozygota w C6677T. Czy powinno mnie to niepokoić?
Mój mail jarek@zespoldowna.info
W jaki sposób można dokonac zbadania genow o których piszesz? Czy badanie ngs WES to wykaze? Wiem że mamy tak jak wyżej mthfr heterozygota A1289C i homozygota w C6677T, zespół marfana, hemochromatoze wrodzona… czy cbs jest zawsze powiązany z mthfr?
https://mthfr-genetics.co.uk/
CBS jest istotnym elementem w metylacji i należy uwzględniać go w jej analizie.